武爱文医生的科普号
- 精选 直肠癌新辅助治疗后非手术治疗展望
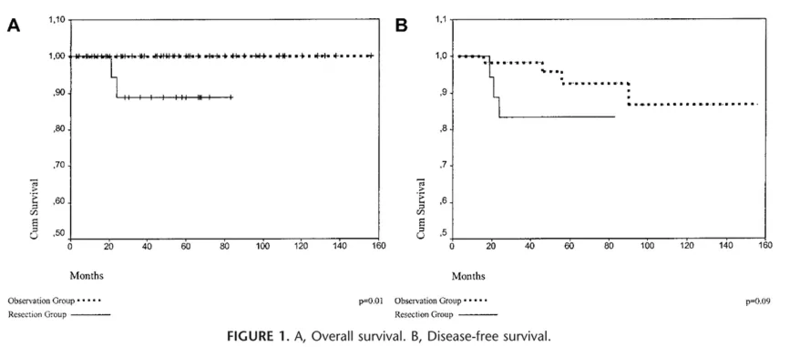
一、新辅助放化疗(NCRT)后“观察等待(watch and-wait)策略”:有证可循对于MRI确定为高危的直肠癌患者,新辅助放化疗(nCRT)是其标准的治疗方式,nCRT对于直肠癌患者的价值在于达到肿瘤降期、提高R0切除率以及肛门括约肌保留率。据相关研究结果显示,直肠癌患者在nCRT后,临床完全缓解率(cCR)最高可达67%,病理学完全缓解(pCR)可达15%~40%。 在生存预后方面,S. T. Martin等对直肠癌nCRT后的结局进行系统回顾和荟萃分析,结果显示,在nCRT后达到pCR的直肠癌患者,其长期生存通常极为良好,5年无疾病生存率(DFS)可高达85%~100%,而局部复发率几乎为0。 二、nCRT后观察等待疗法对比根治手术:孰优孰劣?相对于观察等待而言,nCRT后接受手术治疗存在一定的弊端,例如合并症发生率较高(约占6%~35%),包括出血、败血症及吻合口裂开等;还可能导致一定的长期功能性问题,例如肠道、膀胱及性功能的障碍,从而影响直肠癌患者的生活质量。S. T. Martin等的荟萃分析显示,11%~44%的患者接受了经腹会阴联合切除术(APR)。过去十年,nCRT随后行直肠切除术已经成为局部晚期直肠癌的标准治疗方法,那么,无论nCRT效果如何,直肠癌nCRT后手术治疗是否属于过度治疗?nCRT后是选择观察等待还是手术治疗?一些研究者对此展开了探索。 2004年Ann Surg杂志上的一项研究比较了nCRT后分别接受根治手术和观察等待,旨在比较其对于直肠癌患者生存的影响。结果显示:观察等待组患者的生存期并不劣于根治手术组,其无病生存期(DFS)的差异无统计学意义(P=0.09)。此外,在总体生存期(OS)方面,观察等待组的OS甚至要优于根治手术组(P=0.01)。 2018年武爱文教授团队发表于《中华胃肠外科杂志》的研究探讨了中低位直肠癌新辅助治疗后,评效为cCR或近临床完全缓解(near-cCR)患者实施观察等待疗法或实施器官保留手术的预后,结果显示,cCR组/near-cCR组及同期根治术后病理完全缓解(ypCR)患者的3年肿瘤特异性生存率无统计学差异(100% vs.100% vs. 93.4%,P=0.186)(图2)。 三、观察等待治疗失败:以局部再生为主,可视情况选择挽救治疗2018年Lancet杂志上的一项研究共纳入1009例在NCRT后接受观察等待的直肠癌患者,其中880例患者在nCRT后达到临床完全缓解(cCR)。在中位随访3.3年后,结果发现:①共有213例出现了局部再生(占24.2%),其中136例(64%)发生于第1年内,188例(88%)则发生于2年内。此外,局部再生的部位有97%(206例)位于肠壁,另有3%(7例)位于局部淋巴结。②共有71例患者出现了远处转移,其中44例为肺转移(62%),29例为肝转移(41%),4例为腹膜转移(6%)。而且,研究显示,肿瘤复发有一定的规律。 当观察等待治疗失败后,则需要进行相应的挽救治疗。对于局部再生的结直肠癌患者而言,通常推荐接受手术治疗,而对于远处转移的患者而言,则选择化疗及靶向治疗等。在上述研究中的213例局部再生结直肠癌患者中,148例接受了手术治疗,其中46例为局部切除(13例随后又接受了全直肠系膜切除术[TME]),115例为TME,R0切除率为99%。武爱文教授团队的研究中,初始诊断为cCR的49例患者中,11例(22.4%)发生肿瘤局部再生,其中9例接受了补救性手术:5例接受根治术后无局部复发,4例接受局部切除的患者中1例出现局部复发(图3)。初始诊断为near-cCR的13例患者中,7例接受局部切除,6例患者观察等待。7例接受局部切除的患者中有6例进一步明确为cCR,1例因接受全程新辅助治疗后根据患者意愿进行随诊,局部切除术后患者均未发生局部肿瘤再生。6例接受观察等待疗法的患者中,有4例出现局部肿瘤再生,均接受补救性根治切除(图4)。 四、cCR及pCR:如何评估?直肠癌患者在接受新辅助治疗后肿瘤退缩明显,呈溃疡瘢痕样改变,直肠指检、影像学检査及病理学检査活检无明显肿瘤证据,称为cCR。单纯内镜评估cCR的敏感度低。对于结直肠癌患者而言,目前对cCR的国际公认标准有三点:①肛门指诊原肿瘤区域正常,没有肿瘤性肿块可触及。②内窥镜下可发现白色、扁平的粘膜斑痕,伴周围毛细血管扩张,未见肿瘤性溃疡或结节,粘膜活检为癌细胞阴性。③盆腔高分辨率MRI检测,T2加权图像仅表现为黑的T2信号而没有中等强度T2信号,且无重大的淋巴结征象;DW图像在B800-B1000期间无可视化信号,伴或不伴ADC图上无信号或低信号、肿瘤区域的肠管肠壁表现为均质、线性信号。汇总目前cCR和近cCR评估标准见表1。 就钳夹活检和空芯针穿刺活检对直肠癌nCRT后病理缓解状况的预测价值而言,研究显示,与手术标本的组织病理学比较,钳夹活检的阳性预测值、阴性预测值分别为100%和23.52%,假阴性预测率和精确率分别84.78%、36.07%;空芯针穿刺活检的阳性预测值、阴性预测值分别为100%和44.44%,假阴性预测率和精确率分别29/58%、78.05%。 nCRT后达到pCR的文献报道是15%~30%,部分术后病理pCR的患者仍不符合目前的cCR标准。目前,尚无可靠的方法来准确检测和判断cCR,武爱文教授指出,目前“唯有时间才是最终判断cCR的方法”。例如,经过长时间的随访观察,通过肠镜观察到cCR和近cCR的特征性图像,即可判断。 五、直肠癌患者的观察等待疗法:严密随访必不可少根据北大肿瘤医院的数据,nCRT后非手术治疗的直肠癌患者发生局部再生和远隔转移发生率分别为24.2%和8.0%,与国际报道的数据吻合。局部再生经过挽救性治疗效果极佳,而发生远隔转移的患者采取积极的多学科治疗也可提高生存率。因此,直肠癌患者在进行观察等待疗法时一定要有严密的随访方案,以便及时发现局部再生和远隔转移并采取相应治疗措施。 六、总结近年来,国内外多项研究显示中低位直肠癌放化疗后达到Ccr/near-cCR的患者采取等待观察疗法,远期预后良好,局部再生和远隔转移率低,其生存率与根治手术后pCR患者相似。此外,更强化的nCRT后非手术治疗的探索也在进行中,如PKUCH-R01研究。目前,局部晚期直肠管理策略已经发生改变,随着研究证据的增多,观察等待疗法有望成为新辅助治疗后肿瘤退缩良好的直肠癌患者保留器官功能的一种治疗选择
 武爱文 主任医师 北京肿瘤医院 胃肠肿瘤中心三病区5333人已读
武爱文 主任医师 北京肿瘤医院 胃肠肿瘤中心三病区5333人已读 - 精选 对胃癌手术的几点思考
来源:中国医学论坛报 日期:2011-07-05作者简介:武爱文,2002年获得北京大学医学博士学位,2010-2011年分别前往美国纪念斯隆-凯特林癌症中心和日本国立癌症中心中央病院参观交流。现任北京大学肿瘤医院副主任医师、副教授,中国抗癌协会胃癌专业委员会青年委员会副主任委员。胃癌是全球发病率和死亡率均居高的恶性肿瘤,中国胃癌患者占世界胃癌患者总数的半数以上,可谓是“胃癌大国”,且目前仍未见胃癌发病率有下降的趋势。下面围绕目前胃癌规范化及个体化手术的问题,结合《美国国立综合癌症网络(NCCN)胃癌临床实践指南》等常用指南及临床实践,简单谈谈自己的几点思考,与广大同行共勉。检出淋巴结时间≈手术时间病理检查是胃癌规范化手术有机部分胃癌分期及众多胃癌临床治疗指南均提出要求,胃癌手术淋巴结检出数目应该在15枚以上,以便保证临床分期的确切性。而如果要获取15枚以上的淋巴结,不但外科医生应在手术中清扫必要站别的淋巴结,而且要求病理科医生能检出足够的淋巴结,因此这有待外科与病理科的密切协作,也需要病理科医生的耐心。据悉,早年日本外科医生甚至在手术后花费与手术类似的时间来用于淋巴结的检出。笔者在日本国立癌症中心中央病院交流期间发现,熟练的外科住院医生须花费40分钟来按站别检出30枚以上的淋巴结。而且术中标记淋巴结的具体部位有助于术后淋巴结的分站。在临床上,笔者也经常遇到外院咨询胃癌根治术后治疗方案者,其中清扫淋巴结数目不能达到基本要求者甚多,因此深感将病理科纳入胃癌规范化手术平台的必要性。消化道重建方式→术后生活质量应重视胃的切除范围和重建方法胃癌复发形式包括局部复发、腹膜转移和血行转移。而足够的胃切除范围是减少术后局部复发的重要手段。在ACTS-GC研究中,1059例根治术后胃癌患者的局部复发率约为2%。《NCCN胃癌临床实践指南》建议,胃切缘距离肿瘤边缘应在4~5 cm以上。国内早年研究也发现,不同病理类型胃癌的安全手术切缘有所差异。例如,我们建议对弥漫浸润性胃癌行全胃切除。亚临床局部肿瘤残留、腹腔转移和血行转移是目前临床研究的热点。胃癌患者术后生活质量与其消化道重建方式有直接关系。胃切除术后反流性胃炎、食管炎、胃动力不良等严重影响了患者的消化、吸收功能。而采用不同的消化道重建方式则有助于减少患者术后不适,但这常常被一些外科医师以增加手术风险为由拒绝。笔者认为,在目前外科技术成熟、手术并发症发生率较低的情况下,在进行根治性切除手术的同时,应努力通过外科手段改善患者术后生活质量。我院胃肠外科针对全胃切除术后间置空肠代胃的初步研究也证实,这种处理可改善胃癌患者的生活质量。对术前诊断为Ⅱ型糖尿病者在远端胃大部切除术后尽量采用胃空肠Roux-Y吻合,将有助于控制糖尿病。因此,对于胃癌患者的术后消化道重建,应综合考虑实际情况,慎重作出个体化选择。外科手术≠工业流水线胃癌规范化手术应保证足够手术时间胃癌手术不同于胃大部切除,往往须显露胃周重要血管,清扫周围脂肪淋巴组织。因此良好的显露、正确的解剖层次和确切结扎,可最大限度地减少出血和手术创伤。除了传统手术刀、剪刀外,近年来电外科器械及结扎束、超声刀的使用使出血进一步减少,手术时间进一步缩短。但是,外科手术尤其是规范性的非急诊手术不应一味强调手术速度,而更应该重视手术的规范性,肿瘤手术尤其如此。在手术过程中不断发现新的临床现象,可提高对疾病的认识水平。手术过程中解剖结构的变异,围手术期治疗后组织的变化以及个体化的发现,都是手术区别于工业流水线的重要特点。标准+规范→个体化胃癌淋巴结清扫及个体化治疗肿瘤个体化治疗是未来的发展方向,包括手术、药物治疗及预防等。个体化的前提是标准化,在没有标准化治疗、缺乏令人信服证据的情况下,仅依靠经验开展个体化治疗是盲目的,风险也是较大的。早期胃癌内镜下切除包括黏膜切除和黏膜下层切除,这建立在对早期胃癌转移规律进行过充分研究的基础上,其中超声胃镜的准确分期是必要条件,盲目开展势必延误有效的治疗。同样,胃癌的个体化淋巴结清扫也必须建立在对胃癌个体化转移规律深入认识的基础上。应该讲,中国胃癌患者具有与西方及其他亚洲国家患者都不同的特点。在日本和韩国,近端胃癌及胃食管交界部癌的发生比例不足10%,而中国不少高发地区这一比例高达30%以上,与欧美近似。而且,我国患者在发病原因和临床特点上也与其他国家和地区有很大区别。因此,胃癌治疗的个体化也体现在不同种族、不同人群的治疗策略的差异上。■个人体悟何为真正的规范化手术?在胃癌的治疗中,目前手术仍是最为重要的治疗手段。应该讲,高质量的胃癌手术以清除体内可见病灶是胃癌手术的基础及减少复发和改善疗效的前提。淋巴结转移可较早出现于多数早期、中期胃癌,同时又可通过手术来得以清除,因此对胃癌规范化手术讨论和争议最多的就是淋巴结清扫范围。历经数十年,亚洲、欧美学者围绕胃癌规范化手术的争议终于几近平息,大家在胃癌淋巴结清扫范围上基本达成了共识。《NCCN胃癌临床实践指南》也明确提出,推荐在有经验的胃癌诊疗中心进行胃癌手术,建议清扫胃周及血管周围的淋巴结(即D2淋巴结清扫)。国内学者早在上个世纪80年代即开始倡导D2淋巴结清扫。但遗憾的是,在国内胃癌治疗专科化水平不高的前提下,胃癌规范化手术的观念虽然广为接受,但手术操作中的“规范化”却存在相当大的“个体化”和“随意化”问题。此现象在各级医院的普通外科、胃肠外科、肿瘤外科以及不同的医生中广泛存在。近年来,胃癌规范化培训项目在全国得到广泛开展,使胃癌规范化手术的概念得到强化,手术演示也使规范操作成为可能。笔者认为,胃癌规范化手术是一个系统工程,绝非简单的观念问题,因此在进一步的开展过程中还是应注意和强调几点:病理检查是胃癌规范化手术的有机部分;胃癌规范化手术要保证足够的手术时间;重视胃的切除范围和重建方法;积极开展中国胃癌患者的临床研究;目前胃癌规范化手术的推广和普及是提高全国胃癌治疗水平的基础工作;多学科协作尤其是与病理科的密切合作是规范胃癌手术的有机部分;而在规范化手术的基础上,建立和应用全国性胃癌临床数据库,将是未来中国开展个体化手术等治疗的必要工作。
武爱文 主任医师 北京肿瘤医院 胃肠肿瘤中心三病区1.1万人已读 - 精选 乙状结肠系膜PEComas一例并文献汇总
http://www.xctmr.com/pathology/nb/2009-01-30/1426.html分化未定的肿瘤——具有血管周上皮样细胞分化的肿瘤【定义】 具有血管周上皮样细胞分化特点的肿瘤(PEComas)是由组织学和免疫组化上有独特表现的血管周上皮样细胞构成的间叶性肿瘤。PEComas家族肿瘤包括:血管平滑肌脂肪瘤(AML)、肺透明细胞"糖"瘤(CCST)、淋巴管平滑肌瘤病(LAM)、镰状韧带透明细胞肌黑色素细胞性肿瘤(CCMMT)和少见的发生于胰腺、直肠、腹膜、子宫、阴道、大腿和心脏的透明细胞肿瘤。此类肿瘤的某些类型分别在WHO肾(AML)、肝(AML)、肺(CCST、LAM)肿瘤章节中进行讨论。【同义词】 肺外糖瘤,血管周上皮样细胞肿瘤(PECT),单形性上皮样血管平滑肌脂肪瘤【流行病学】 非AML、CCST和LAM的PEComas相当罕见,目前只有大约31例报道。 CCMMT一般发生在年轻女孩,诊断时平均年龄11岁。子宫PEComas的平均诊断年龄是54岁。报道的其他PEComas几乎全部为女性,发病年龄广。【受累部位】 报道的PEComas发生于子宫13例,镰状韧带8例,大肠和小肠3例,胰腺、盆腔侧壁、阴道、大腿和心脏各1例。【临床表现】 CCMMT表现为有疼痛的腹部肿物,子宫PEComas可以出现阴道出血,其他PEComas的典型表现是无痛性肿物。非AML、CCST和LAM的PEComas不伴有结节性硬化综合征。【组织病理学】 血管周上皮样细胞(PECs)的特征是位于血管周围,常在血管腔周围放射状排列。典型表现是:大多数紧邻血管周围的PECs为上皮细胞样;离血管较远的呈梭形类似平滑肌细胞。上皮样细胞和梭形细胞的相对比例有较大差异。PECs胞质透明至颗粒状、微嗜酸,与真正的平滑肌细胞的深染嗜酸性胞质不同。典型细胞的核小、中位、圆形或椭圆形、染色质密度中等、核仁小,但也可见明显深染的不规则核。 大多数PEComas类似CCST,PEC排列在薄壁血管周围。很大一部分PEComas细胞核有明显异型性,核分裂象多,有坏死。子宫PEComas可呈浸润性生长,类似于低级别子宫内膜间质肉瘤。CCMMT与其他PEComas有些不同,几乎全部由梭形细胞构成,细胞大小一致、中等大小、排列成束状和巢状。一个显著特征是有精细的血管网,小的弓形血管将肿瘤分隔为粗糙团块状,类似肾细胞癌。分裂活性、血管淋巴管侵及和坏死未见报道。【免疫表型】 黑色素细胞标记物阳性是PEC的特征,如HMB45、MelanA、酪氨酸酶、小眼转录因子(microphthalmia转录因子)、NKI/C3。肌标记物阳性,如SMA、pan-muscle actin、musclemyosin和肌钙蛋白。desmin阳性不常见,角蛋白和S-100一般阴性。PEComas最敏感的黑色素细胞性标记物是HMB45、MelanA和小眼转录因子。【超微结构】 胞质内有丰富的糖原、前黑色素小体、细微丝、偶尔有致密小体、半桥粒和形成不良的细胞间连接。【遗传学】 据报道,1例CCMMT有t(3;10)(9p13;9q23)。其他PEComas尚未进行细胞遗传学和分子遗传学研究。少数CCMMT同时有结节硬化相关的TSC2基因产物tuberin表达缺失。【预后因素】 因为罕见,所以尚无明确的恶性PEComas诊断标准,况且最常见的PEComas-AML内常见假恶性变,使标准更难确定。但是,临床表现为恶性的(即转移性)AML已有明确记载(常为上皮样),并与报道的多种非AML、LAM和CCST型PEComa相当类似。同样有良性AML发展为肉瘤的报道。此外,临床表现为恶性的肺CCST,以及发生于小肠、子宫和心脏的恶性PEComas也有报道。根据目前报道,有浸润性生长、细胞明显丰富、核增大并且深染、分裂活性高、非典型性核分裂和凝固性坏死的PEComas应视为恶性。恶性PEComas是具有侵袭性的肉瘤,常导致患者死亡。目前看来,与其他PEComas相比,CCMMT是一种相对良性的病变。[治疗]外科是唯一可能治愈的方法。放化疗未见明显效果。但总体例数很少,故很难进行临床研究和观察。但最近Kenerson et al. 报告此类肿瘤TSC1/2 失活和m-TOR激活提示可能针对此现象的针对性治疗包括m-TOR可能会显效。Kenerson H, Folpe AL, Takayama TK, Yeung RS (2007) Activation of the mTOR pathway in sporadic angiomyolipomas and other epithelioid cell neoplasms. Hum Pathol 38:1361–1371.
武爱文 主任医师 北京肿瘤医院 胃肠肿瘤中心三病区4112人已读 - 精选 体检
肿瘤普查当作哪些检查肿瘤疾病的高发让肿瘤的预防和治疗成为热门,人们在感伤于名人因肿瘤英年早逝之余也在积极需求更好的早诊措施。于是乎,肿瘤的普查和体检成为当下体检中心和很多医疗结构的重要工作之一。那么,究竟肿瘤的普查有什么问题和误区,又应当做什么检查呢?很多人把肿瘤的普查等同于血液肿瘤标志物检查,如CEA、CA199、CA72.4、CA125、AFP等。不可否认,上述肿瘤标志物对早期针对会有一定帮助,如AFP对筛查原发性肝细胞癌颇有意义,近1/3的胃肠道肿瘤患者CEA阳性,其它血液肿瘤标志物也会在肿瘤早期有不同程度的升高。但除了AFP外,恶性肿瘤早期出现血液肿瘤标志物升高的比例并不高。也就是讲,血液肿瘤标志物检查正常不代表没有肿瘤。另外一个问题是,血液肿瘤标志物升高是否代表肯定有肿瘤呢?笔者在门诊经常遇到因此问题而咨询者。肿瘤的诊断必须有影像学和病理学的证据,单纯依靠血液肿瘤标志物升高诊断肿瘤是不够的。我们往往会根据不同血液肿瘤标志物的升高情况选择最可能得出阳性结果的检查手段。多年前曾遇到一例因血液CA153升高发现乳腺癌者,至今仍记忆犹新。像AFP的升高除见于肝癌外,还见于少数胃癌、畸胎瘤、胚胎源性肿瘤、肝炎等。CA199的升高可见于很多消化道肿瘤,多囊胰的病例中也有CA199显著升高者,而非仅见于胰腺癌。一言概之,血液肿瘤标志物的升高仅仅起到提示作用,是一条线索,是一根藤,但顺藤摸到的未必是瓜,可能是叶。笔者认为,体检中应该更为重视的是主诉,即自我感觉到的不适。常见的提示肿瘤发生的是不明原因的出血、消瘦、炎症、肿块等,任何年龄的人群、在任何部位出现上述情况都应该引起足够重视。目前体检系统中“重仪器、轻问诊和查体”的现象很容易出现漏诊。一般的体检项目中对肿瘤仅仅是血液检查显然远远不够。中国发病和死亡率居前的肿瘤包括肺癌、胃癌、肝癌、乳腺癌、结直肠癌、食管癌、子宫颈癌等。就目前中国人群中高发的肿瘤种类而言,血液肿瘤标志物仅AFP有早诊意义,宫颈涂片对早期检查子宫颈癌颇有价值,消化系统肿瘤包括胃癌、食管癌、结直肠癌等通过大便潜血、CEA等检查早期效率很低,通过胸部X线检查发现的肺癌往往已是晚期。实际上,上述肿瘤早期也会表现出一定的不适,如刺激性咳嗽、轻度咯血、进食后哽咽感或胸骨后疼痛不适、上腹部不适、便血等。早期的症状结合影像和血液检查有助于提高检出率。受检者的心态是求阴性,如为阴性则如释重负,但如为假阴性则会贻误病情;检查者应抱求阳性心态,减少漏诊。体检过程中也应该询问家族病史,以便发现遗传性或高危患者。需要提醒的一点是,体检结果只能作为参考。不少单位设计了不同的体检套餐,豪华者包括诸如PET-CT、生物芯片在内的新手段。肿瘤的种类很多,目前所涉及的体检尚不能完全涵盖,体检的手段亦有一定的局限性,敏感性并非百分之百。因此,参加体检千万不能为宣传中的噱头所迷惑,谨慎关注自己的身体变化是最为重要的。那体检应该做哪些检查呢?首先,应向主检医生介绍自己的顾虑、不适和既往病史,如担心可能会出现什么类型的肿瘤、自己身体微小的变化和不适,会提示医生做针对性的体检。如有多年乙肝病史,那肝脏的针对性检查是很必要的。其次,不拒绝查体,尤其是暴露性查体和肛门指诊,有些发现往往是意外的发现。中国人大肠癌中大多数为直肠癌,多为中低位,是通过肛门指诊可以查到的。血液学检查,包括AFP、CEA等检查结果会对进一步的影像检查有提示作用。再次,有针对性的或间断性的进行影像学检查,如胃镜、肠镜、CT乃至于PET-CT检查。在美国部分地区已经批准通过胸部CT扫描来对肺癌进行普查,虽然会增加人体接受的辐射量,但肺癌的检出效率显著提高。总之,体检是早期发现肿瘤的重要手段,但也是一个复杂的甄别过程。在这个过程中,受检者的积极参与包括对自身不适的叙述尤为重要,全面的体格检查也是非常关键的,恰当的辅助检查是必要的补充。
武爱文 主任医师 北京肿瘤医院 胃肠肿瘤中心三病区4625人已读 - 精选 胃肠道间质瘤诊治进展
武爱文胃肠道间质瘤(Gastrointestinal stromal tumor,胃肠道间质瘤)以前是指来自胃肠道和腹膜间叶组织包括平滑肌、神经组织等的肿瘤,是多种肿瘤的集合体,包括平滑肌瘤、平滑肌肉瘤、雪旺细胞瘤等。除外科手术外,缺乏有效的治疗手段。[1-3] 1998年Hirota等发现绝大多数的胃肠道间质瘤存在c-kit基因的突变,[4] c-kit基因编码跨膜酪氨酸激酶受体,配体为干细胞因子,受体和配体的相互结合是黑色素细胞、红细胞、生殖细胞、尘细胞和Cajal细胞发育所必需的。[5-9] 而Cajal细胞的表型与胃肠道间质瘤极为相似,提出胃肠道间质瘤来源自胃肠道的Cajal细胞。[4] 2002年临床试验报告分子靶向药物甲磺酸依马替尼(商品名为格列卫)治疗复发和转移性胃肠道间质瘤有效率高达80%,[10] 大大改变了胃肠道间质瘤的治疗现状,该药物是c-kit的特异性抑制剂。至此,胃肠道间质瘤的治疗状况以及对其组织发生机制的认识有了革命性的改变。目前胃肠道间质瘤被定义为原发于胃肠道和腹腔的间叶细胞肿瘤,细胞为梭形或上皮样,免疫组织化学c-kit染色阳性。[11,12] 胃肠道间质瘤C-KIT阳性,表现为胞浆内弥漫着色,通常90%以上的肿瘤细胞均阳性,约50%病例胞浆着色呈点状,但也常与弥漫着色并存。少于25%细胞着色不多见,由此可见方法操作正规是不难确定的。吴秉铨强调在组织取材时要包括正常肠组织,其中正常存在的肥大细胞可用做阳性对照。[13] 以前认为该肿瘤较为少见,发病率约为20-40/100000,占全部胃肠道肿瘤的1%,占全部肉瘤病例的5-10%。最近瑞典Nilsson 等报告胃肠道间质瘤(按照最新定义)发病率可达14.5/100000/年。在国内尚缺乏有关的流行病学报告。胃肠道间质瘤可发生于消化道任何部位,包括口腔、食管、胃、小肠、结肠、直肠和肛门、腹膜等。最多见于胃(占60-70%),其次为小肠,约占25-35%,其它部位罕见。虽然绝大多数胃肠道间质瘤表达c-kit,但也有部分c-kit阴性者,约占5%。[14] 已经发现c-kit基因分别有9、11、13、17等外显子的突变异常,约占胃肠道间质瘤的80%病例。2003年Fletcher等报道了c-kit野生型胃肠道间质瘤具有血小板衍生生长因子受体A (PDGFRA) 的基因突变,约占胃肠道间质瘤病例的7%。[15-17] 有研究发现,35%的c-kit表达阴性患者有PDGFRA基因的突变。[15] C-kit 和PDGFRA基因突变的肿瘤有不同的信号通路,介导不同途径的信号传导通路和细胞遗传学改变。Tzen CY等对108例胃肠道间质瘤进行筛查,发现其中7例(6%)为c-kit阴性,并且全部7例均有c-kit基因的突变、PDGFRA为野生型。在外显子557/558位点突变的c-kit阴性间质瘤核分裂像较多,多>10/50个高倍视野,其中75%随访出现多发转移和复发。[14] 可见两个基因的突变有可能导致胃肠道间质瘤生物学行为的改变。Lasota等认为大多数PDGFRA突变的胃间质瘤恶性程度较低,细胞形态多为上皮样。[18] 目前认为,无论大小、部位,胃肠道间质瘤都有一定的恶性倾向。根据肿瘤大小和核分裂像数目将胃肠道间质瘤分为极低恶性、低度恶性、中度恶性和高度恶性四类,便于患者的预后判断。[19,20] 比较公认的指标是肿瘤大小和组织学上核分裂像数目。肿瘤直径能够缩小肿瘤,提高手术切除率。格列卫是一种酪氨酸受体抑制剂,能特异性结合c-kit。在体外、体内和细胞水平都可强烈抑制酪胺酸激酶的活性,是干细胞因子(SDCF) 受体kit的强抑制剂。格列卫口服后经肝脏P450 酶转换为CYP3A4/ 3A5,主要经肠道排出,7 天内几乎完全排泄。[26] 沈琳等报告采用格列卫治疗30例胃肠道间质瘤患者,剂量为200-600mg/日,有效率为58.3%。[27] 格列卫治疗尚无统一剂量标准, 一般推荐400mg/天,使用较安全且疗效肯定,出现耐药或疾病进展后可提高剂量。有研究发现,在上述剂量无效或者进展的患者提高药物剂量,仍然可以显效。[28-29] 我国目前也在进行临床研究,剂量较欧洲研究剂量偏小,但疗效肯定。格列卫的常见副作用为水肿、恶心呕吐、腹痛、乏力、皮疹或皮肤潮红以及出血。多为轻、中度。总体看,该药安全性较好。[28] 格列卫治疗胃肠道间质瘤可谓近年来分子靶向治疗的重大进步。但是,并未解决这一问题的全部。如对格列卫原发/继发耐药、治疗中断后疾病进展以及辅助核和新辅助治疗等课题正在等待进一步临床研究结果的出现。[30-32] 其他,还需要探索的是,是否可以和传统的化疗药物有选择的进行联合治疗,或与其他靶向治疗药物联合。其他诸如放射治疗、免疫治疗尚无证据说明其有效性,临床一般不予采用。有关胃肠道间质瘤的预后因素,目前认为包括诊断时的病期、肿瘤大小、核分裂像计数、外科手术、c-Kit和PDGFA的基因突变、是否使用格列卫以及使用方法等。[33-35] 目前也有研究探讨胃肠道间质瘤其他分子标志物表达的价值所在。参考文献:1. Miettinen M, Lasota J. Gastrointestinal stromal tumors (GISTs): definition, occurrence, pathology, differential diagnosis and molecular genetics. Pol J Pathol. 2003;54:3-242. Pidhorecky I, Cheney RT, Kraybill WG, Gibbs JF. Gastrointestinal stromal tumors: current diagnosis, biologic behavior, and management. Ann Surg Oncol. 2000;7(9):705-12. 3. Casper ES. Gastrointestinal stromal tumors. Curr Treat Options Oncol. 2000;1:267-734. Hirota S, Isozaki K, Moriyama Y, et al. Gain-of-function mutations of c-kit in human gastrointestinal stromal tumors. Science 1998, 279, 577-580.5. Blume-Jensen P, Claesson-Welsh L, Siegbahn A, Zsebo KM, WestermarkB, Heldin CH: Activation of the human c-kit product by ligand-induced dimerization mediates circular actin reorganization and chemotaxis. EMBO J 1991, 10, 4121-4128.6. Chabot B, Stephenson DA, Chapman VM, Besmer P, Bernstein A: The protooncogene c-kit encoding a transmembrane tyrosine kinase receptor maps to the mouse W locus. Nature 1988, 335, 88-89.7. Lev S, Blechman J, Nishikawa S, Givol D, Yarden Y: Interspecies molecular chimeras of kit helps define the binding site of the stem cell factor. Mol Cell Biol 1993, 13, 2224-2234.8. Williams DE, Eisenman J, Baird A, Rauch C, van Ness K, March CJ, Park LS, Martin U, Mochizuki DY, Boswell HS et al: Identification of a ligand for the c-kit protooncogene. Cell 1990, 63, 167-174.9. Zsebo KM, Williams DA, Geissler EN, Broudy VC, Martin FH, Atkins HL, Hsu RY, Birkett NC, Okino KH, Murdock DC et al: Stem cell factor is encoded at the S1 locus of the mouse and is the ligand for the c-kit tyrosine kinase receptor. Cell 1990, 63, 213-224.10. Demetri GD, von Mehren M, Blanke CD, van den Abbeele AD,Eisenberg B, Roberts PJ, Heinrich MC, Tuveson DA, Singer S, Janicek M, Fletcher JA, Silverman SG, Silberman SL, Capdeville R, Kiese B, Peng B, Dimitrijevic S, Druker BJ, Corless C, Fletcher CD, Joensuu H: Efficacy and safety of imatinib mesylate in advanced gastrointestinal stromal tumors. N Engl J Med 2002, 347, 472-480.11. Miettinen M, Lasota J. Gastrointestinal stromal tumors-definition, clinical, histological, immunohistochemical, and molecular genetic features and differential diagnosis. Virchows Arch 2001; 438:1-1212. Miettinen M, Majidi M, Lasota J. Pathology and diagnostic criteria of gastrointestinal stromal tumors (GISTs): a review. Eur J Cancer 2002; 38(suppl5): 39-5113. 吴秉铨。胃肠道间质瘤诊断病理的商榷。广东医学 2004;25(3):232-23314. Tzen CY, Mau BL. Analysis of C-KIT-negative gastrointestinal stromal tumors. World J Gastroenterol. 2005 Feb 21;11(7):1052-5.15. Heinrich MC, Corless CL, Duensing A, McGreevey L, Chen CJ, Joseph N, Singer S, Griffith DJ, Haley A, Town A, Demetri GD, Fletcher CD, Fletcher JA: PDGFRA activating mutations in gastrointestinal stromal tumors. Science 2003, Jan 9 [epub ahead of print]. 16. Heinrich MC, Rubin BP, Longley BJ, Fletcher JA: Biology and genetic aspects of gastrointestinal stromal tumors: KIT activation and cytogenetic alterations. Hum Pathol 2002, 33, 484-495.17. Fletcher JA, Fletcher CDM, Rubin BP, Ashman LK, Corless CL, Heinrich MC: KIT gene mutations in gastrointestinal stromal tumors. More complex than previously recognized? Am J Pathol 2002, 161, 737-738. 18. Laboratory Investigation 2004;84:874-883。19. Miettinen M, El-Rifai W, Lasota J, Sobin LH: Evaluation of malignancy and prognosis of gastrointestinal stromal tumors: a review. Hum Pathol 2002, 33, 478-483.20. Fletcher CD, Berman JJ, Corless C, Gorstein F, Lasota J, Longley BJ, Miettinen M, O'Leary TJ, Remotti H, Rubin BP, Shmookler B, Sobin LH, Weiss SW. Diagnosis of gastrointestinal stromal tumors: A consensus approach. Hum Pathol. 2002 May;33(5):459-65. Review.21. Buckley JA , et al. Radiographics 1998 ; 18(2) : 379 - 392. 22. Burkill GJC, Badran M, Al-Muderis O, et al. Malignant gastrointestinal stromal tumors: distribution, imaging features, and pattern of metastatic spread. Radiology 2003; 226:527-53223. Roberts PJ, Eisenberg B. Clinical presentation of gastrointestinal stromal tumors and treatment of operable disease. Eur J Cancer 2002; 38: S37-3824. Dematteo RP ,Heinrich MC ,El2Rifai WM ,et al . Clinical Management of gast rointestinal st romal tumors :before and after STI571. Hum Pat hol ,2002 ,33(5) :46625. 卢震海,万德森。胃肠道间质瘤的外科治疗。广东医学。2004;25(3):233-23526. 曹宝山。胃肠道基质细胞瘤诊治进展。实用癌症杂志。2004;19:208-21027. Demetri GD, von Mehren M, Blanke CD, et al. Efficacy and safety of imatinib mesylate (STI571) in advanced gastrointestinal stromal tumors. N Engl J Med 2002; 347:472-48028. P Bu mming ,J Andersson. Neoadjuvant ,adjuvant and palliative treatment of gast ro2intestinal st romal tumours ( GIST) wit h imatinib : a cent re2based study of 17 patients. British Journal of Cancer ,2003 ,89 (3) :460.29. Nishida T, Yasumasa K. [Target-based therapy against gastrointestinal stromal tumors--from molecular diagnosis to molecular target therapy] Gan To Kagaku Ryoho. 2003 Aug;30(8):1071-8. Review. Japanese.30. Verweij J, van Oosterom A, Blay JY, Judson I, Rodenhuis S, van der Graaf W, Radford J, Le Cesne A, Hogendoorn PC, di Paola ED, Brown M, Nielsen OS. Imatinib mesylate (STI-571 Glivec(R), Gleevec) is an active agent for gastrointestinal stromal tumours, but does not yield responses in other soft-tissue sarcomas that are unselected for a molecular target. Results from an EORTC Soft Tissue and Bone Sarcoma Group phase II study. Eur J Cancer. 2003 ep;39(14):2006-11.31. Tuveson DA ,Willis NA ,J acks T ,et al . STI571 inactivation of t he gast rointestinal st romal tumor c2KIT oncoprotein :Biological and clinical implications〔J 〕. Oncogene ,2001 ,20 (36) :5054.32. Yan H, Marchettini P, Acherman YI, Gething SA, Brun E, Sugarbaker PH. Prognostic assessment of gastrointestinal stromal tumor. Am J Clin Oncol. 2003 Jun;26(3):221-8.33. Bates AW, Feakins RM, Scheimberg I. Congenital gastrointestinal stromal tumour is morphologically indistinguishable from the adult form, but does not express CD117 and carries a favourable prognosis. Histopathology. 2000 ct;37(4):316-22. Review.34. Ernst SI, Hubbs AE, Przygodzki RM, Emory TS, Sobin LH, O’Leary TJ: KIT mutation portends poor prognosis in gastrointestinal stromal/smooth muscle tumors. Lab Invest 1998, 78, 1633-1636.35. Fletcher JA, Fletcher CDM, Rubin BP, Ashman LK, Corless CL, O’Leary T, Ernst S, Przygodzki R, Emory T, Sobin LH: Loss of heterozygosity at 1p36 predicts poor prognosis in gastrointestinal stromal/smooth muscle tumors. Lab Invest 1999, 79, 1461-1467.
武爱文 主任医师 北京肿瘤医院 胃肠肿瘤中心三病区7373人已读 - 精选 直肠间质瘤
直肠的肿瘤主要来源于粘膜上皮,即前面所述之直肠癌,而来源于间叶组织包括脂肪、肌肉、粘膜相关淋巴组织、血管内皮等的肿瘤少见。我院总结1995年1月至2002年6月间收入的直肠间叶组织来源肿瘤共12例,占
武爱文 主任医师 北京肿瘤医院 胃肠肿瘤中心三病区2.3万人已读 - 精选 胃癌新辅助化疗进展2009
武爱文,徐光炜 [1]浏览近年胃癌领域文献,易知围手术期化疗乃胃癌研究领域之热点。所谓围手术期化疗(perioperative chemotherapy)含新辅助化疗和术后辅助化疗,新辅助化疗(neoadjuvant chemotherapy)亦称术前化疗,旨在缩小肿瘤,提高手术切除率,控制微转移,改善治疗效果。[1] 本文限于篇幅,以评述新辅助化疗现状和进展为主。一、 胃癌新辅助化疗现状和趋势从近年有关胃癌新辅助化疗文献,[2-4]笔者总结此类研究有三大趋势,分述如下。 治疗领域扩大化胃癌新辅助化疗适应证渐宽,从初始时将不可切除之胃癌使其可切除者,而今已延及晚期转移性胃癌,包括肝转移和腹膜转移者,此又得益于目前化疗药物较高的有效率和良好的耐受性之故。围手术期化疗的价值业已得到学界的认可,源于Cunningham牵头的MAGIC研究。[5] 该研究随机入组503例可切除的胃、胃食管结合部和食管下段腺癌,单纯手术组250例,围手术期治疗组253例,所用化疗方案为ECF方案(表阿霉素 50mg/m2 d1,顺铂 60mg/m2 d1,氟尿嘧啶 200mg/m2 d1-21,每21天重复,共三个周期),主要研究终点为总生存率。结果表明两组术后并发症发生率无显著差异,围手术期化疗可显著提高患者无病生存率(HR=0.66)和总生存率(HR=0.75,五年生存率分别为36%和23%),故此治疗模式已成为欧洲进展期胃癌治疗的标准。然该研究存在两个缺陷,一是术前化疗后并未评效,而在术后辅助化疗中仍继续使用原方案;二是研究中纳入了胃、胃食管结合部和食管下段腺癌,此三者实各有异,将此研究结果完全推及到所有胃癌患者似也欠妥。[6] 国内学者回顾性报告87例胃癌患者,有效率为51.7% (15/29),新辅助化疗组与单纯手术组的中位生存期分别为20.6个月和19.9个月(P=0.02),当可亦为佐证。近半数进期期胃癌常出现腹膜转移,一般认为已失去手术机会,效果很差,但近日本针对腹膜转移采用以S-1为主的化疗,长期控制甚至达pCR者个案报告甚多,[7] 值得进一步探讨。对胃癌肝脏转移者也有新辅助化疗之探讨,合理确定适应证,或能使患者获益。治疗模式多样化胃癌围手术期治疗模式目前呈多样化态势,静脉化疗、放化疗结合以及局部动脉灌注化疗等,尤以前两者应用最为广泛。静脉化疗典范当推MAGIC研究,而放化疗结合者的代表则为RTOG9904研究。[8] 该研究方案为氟尿嘧啶、亚叶酸钙和顺铂两周期后同步放化疗(氟尿嘧啶持续滴注并紫杉醇每周输注),结果发现49例患者中病理学完全缓解率甚高,达26%,获得病理缓解的患者1年生存率有改善(82%比69%)。Stahl等新近报告了胃食管结合部腺癌术前化疗与术前放化疗结果的比较。[9] 该临床研究纳入标准为局部进展期(uT3-4NXM0)的食管下段和贲门癌。术前化疗组为化疗15周后手术切除,术前放化疗组为化疗12周后放化疗3周后手术切除,主要终点指标为总生存时间,该研究拟入组354例患者,因入组慢而提前结束,入组的126例患者(119例可评价)中手术切除率相近,放化疗组出现病理学完全缓解者众((15.6% 比2.0%)),淋巴结阴性率高((64.4% 比37.7%) ,3年总生存率高(HR=0.67, 47.4%比27.7%),惟术后病死率略高(10.2% v 3.8%; P =0.26)。我单位近年开展以奥沙利铂为主的新辅助化疗,术后病理学完全缓解者约4%,与此报告相若。可见,术前放化疗也可用于胃食管结合部腺癌,但会增加手术后并发症,包括吻合口漏、腹腔感染的机率。新辅助介入治疗化疗治疗胃癌由来已久,通过高选择性动脉插管将药物注入肿瘤血管,局部药物浓度高,可使肿瘤显著缩小,惜尚缺乏可信度高的大样本研究结果。[10]疗效预测个体化肿瘤的个体化治疗一直是重要的研究方向,胃癌围手术期治疗同样面临着疗效预测的问题,直接影响着治疗的决策。文献报告围手术期治疗显效者预后多较好。Mansour等对168例接受新辅助化疗和R0切除的胃癌患者进行分析,范围组织学有坏死变性或纤维化炎症改变的范围达50%以上者3年疾病特异性生存率(DSS)达到69%,淋巴结转移、pT3及以上、高组织学分级、脉管神经侵犯和组织学改变
武爱文 主任医师 北京肿瘤医院 胃肠肿瘤中心三病区5243人已读





